无菌原料药粉碎机SIP案例应用介绍
2026-01-23

Part.01

Part.02
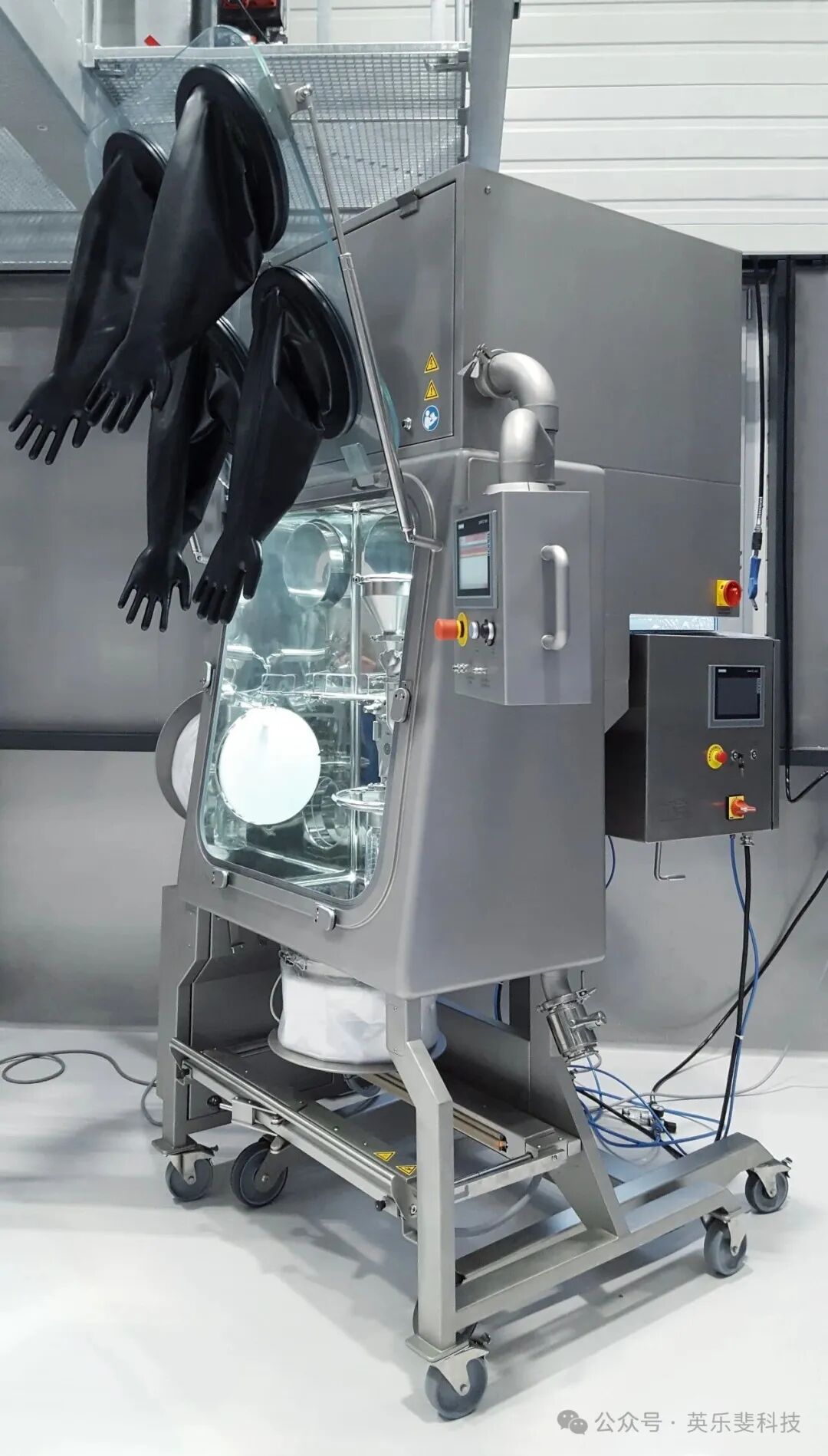

Part.03

联系人
苏先生 150 1922 7346
朱先生 185 0304 7967
咨询热线
0755-8521 3356
传真
0755-8521 3356


Part.01

Part.02


Part.03