无菌隔离器保压测试与手套检漏的合规实施要点
2026-03-13

预处理:关闭隔离器所有门体、阀门及传递口,确保系统处于完全密封状态,断开与外界的非必要连接; 加压与保压:通过内置或外接气源,将舱体加压至验证确定的测试压力(常用100+Pa),稳定后停止供气,启动密封计时; 数据记录:连续记录10~20分钟内的压力变化,同步检查压差报警系统是否正常响应; 合格判定:压力衰减速率需符合企业验证标准,一般要求≤0.5%~1%/min,或遵循ISO 10648-2相关规定,且无异常压力骤降现象。 
定期测试:严格遵循法规及企业CCS文件规定,日常生产用隔离器每季度开展1次全面保压测试,测试需同步记录压差梯度稳定性及报警功能响应情况;年度再验证时必须纳入核心测试项目,结合HEPA过滤器检漏、微生物监测同步进行,全面验证隔离器整体屏障性能,符合YY/T 0567.6—2022及ISO 14644-7相关要求。基于风险评估,高负荷运行、高风险产品(如ADC药物、细胞治疗产品)生产用隔离器,可将定期测试频次提升至每月1次;低使用率且历史性能稳定的隔离器,经风险评估后可适当延长,但最长不得超过6个月,且需在CCS中明确说明依据并留存评估记录。 触发式测试:出现以下情况需立即开展保压测试,合格后方可恢复使用:更换门密封条、维修箱体、更换HEPA过滤器等关键部件后;隔离器发生泄漏报警、压力异常波动等故障,维修完毕后;隔离器安装场地变更、软件升级或运行程序调整后;隔离器长时间停用(超过1个月),重新启用前,需通过保压测试确认舱体密封性能无异常,契合《中国药典》9206及EU GMP附录1对设备维护后验证的要求。 特殊场景测试:无菌检查用隔离器,需在每次无菌检查周期开始前及结束后,额外增加1次保压测试,确保检验过程中隔离屏障的完整性,符合《中国药典》9206及相关验证指导原则要求;冻干制剂分装、无菌灌装等高污染风险生产场景,除常规定期测试外,每批次生产开始前需追加1次保压测试;隔离器进行CD/CV灭菌验证前后,需同步开展保压测试,确认舱体密封性能符合灭菌工艺要求,避免灭菌剂泄漏或外部污染侵入。 再验证相关测试:隔离器全面再验证周期通常为每年1次,若高风险场景或历史偏差较多,可缩短至每6个月1次,再验证过程中需进行至少3次连续保压测试,确保参数重现性与稳定性;期间核查时,需每6个月开展1次简易保压测试,重点监测压力衰减速率,及时发现潜在密封隐患,所有测试数据需纳入质量管理体系,确保可追溯,符合ICH Q9质量风险管理理念及CCS文件要求。

前置检查:每次使用前及高风险操作后,先进行目视检查,确认手套无破损、老化、粘连等明显缺陷; 仪器测试:将手套检漏仪与手套法兰密封连接,根据手套规格设定测试参数(测试压力0.1~0.3MPa,保压时间≥120秒);启动测试后,仪器自动充气并监测压力衰减,记录测试数据; 合格判定:压力衰减值符合设备说明书与企业验证标准,无泄漏报警即为合格;测试数据需纳入电子记录,满足21 CFR Part 11审计追踪要求。 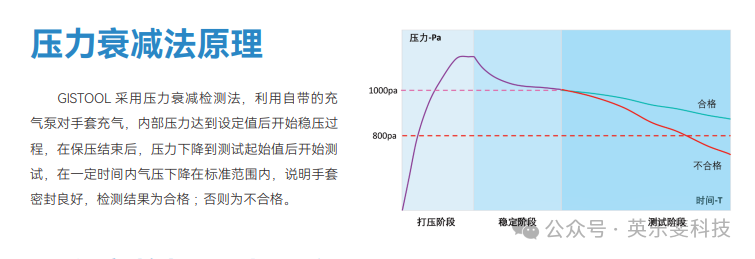
常规频次:每批次或阶段性生产的开始与结束时,必须进行手套检漏仪测试;连续生产的批次间,可通过目视检查替代仪器测试; 高风险场景:冻干制剂分装、无菌灌装等高污染风险操作,需在生产前、中途暂停时、生产后各进行1次仪器测试;手套接触针头、玻璃碎屑等尖锐物品后,立即追加1次测试; 触发式频次:更换手套、维修袖套组件后,需立即进行仪器测试;无菌检查用隔离器需在每次检查周期前后完成测试; 定期复核:每月对所有手套进行1次全检,结合风险评估结果调整测试频次。

 EN
EN



